1前言
眾所周知��,循環(huán)水已用于石油����、化工、鋼鐵等各行各業(yè),在循環(huán)水的使用中����,由于水質(zhì)的不同,會形成各種沉積物�,這些沉積物以無機鹽為主,成為無機垢����;而在有機物的使用或生產(chǎn)過程中,由于高溫等因素的影響����,經(jīng)常會導(dǎo)致有機垢的形成;在有些地方�,則會同時形成無機垢和有機垢。
垢的形成����,會給生產(chǎn)和安全帶來一系列影響����,主要表現(xiàn)四:①影響生產(chǎn)的正常運行。嚴(yán)重的污垢沉積�,使生產(chǎn)設(shè)備的性能下降,甚至不能正常運行;
②增加成本�����。一般地����,污垢的形成使熱交換率大幅度降低,能耗明顯增加���;③引發(fā)各種事故��,原材料泄露�����,引起廠房及工作人員的損傷�。④影響材料性能和設(shè)備壽命�,金屬的污垢,如吸濕性的塵土和無機鹽����,容易吸附空氣中的腐蝕性氣體,如二氧化硫����、二氧化碳��,硫化氫等�����,進而腐獨金屬的表面��,使金屬失去光澤�,產(chǎn)生麻點�����,強度下降����;污垢下會發(fā)生腐蝕,縮短設(shè)備的壽命����。
本文對各種常見無機垢和有機垢的形成機理�、清洗方法進行全面評述
2無機鹽垢的形成及清洗
2.1碳酸鹽垢
2.1.1碳酸鈣垢的成因
以碳酸鈣和碳酸鎂為主要成分,碳酸鎂容易水解生成堿式碳酸鎂���,進而形成溶解度更低的氯氧化誤在天然水中��,鈣的含量夫于鎂��,所以碳酸鹽垢的主要成分為碳酸號�����,有少量的碳酸錢和氧氧化鎖碳酸鹽水垢一般為自色片狀物當(dāng)含有金屬氧化物時�����,會帶有顏色����,如有鐵銹時,早粉紅色或紅褐色它難溶于與冷水����,也難溶于熱水,但易溶于無機強酸��,如鹽酸�����、硝酸和高氯酸等。在工業(yè)用水中存在著各種離子�,有Ca2+、HCO3-�、Mg2+存在時,在受熱條件下發(fā)生下列反應(yīng):
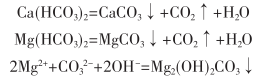
在堿性條件下:
Ca(HCO3)2+2OH-=CaCO3↓+CO32-+2H20
生成碳酸鈣沉積在管壁上形成了碳酸鈣垢����。
2.1.2 清洗機理及方法
碳酸鈣為強堿弱酸鹽,易與強酸發(fā)生復(fù)分解反應(yīng)而溶解����,所以工業(yè)上一般采用廉價的鹽酸添加緩蝕劑如苯胺、烏洛妥品等清洗碳酸鹽垢��。發(fā)生的主要反應(yīng)為:
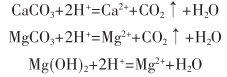
近年來����,人們往往將多種技術(shù)聯(lián)合用于工業(yè)循環(huán)水的清洗,一般采用兩個步驟即首先投用殺菌劑剝離粘泥�����,然后清洗除垢�����!
2.2硫酸鹽垢
2.2.1硫酸鹽垢的成因
硫酸鹽垢的主要成分是硫酸鈣��,有時含有少量的硫酸鎂和氫氧化鎮(zhèn)����,硫酸鈣在水中的溶解度比較小,但較碳酸鈣大的多在40℃以上����,其溶解度隨溫度的升高而略有降低,屬于反常溶解度�����,這一點要特別注意����。硫酸鈣溶解度與溫度的關(guān)系見表1。
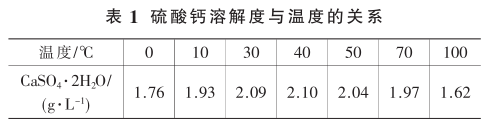
水中含有較高的Ca2+���、SO42-時����,發(fā)生下列反應(yīng):
Ca2++SO42-=CaSO4↓
生成的硫酸鈣沉積在設(shè)備及管道上�,就形成了堅硬致密的硫酸鈣垢�����。
2.2.2清洗機理及方法
(1)轉(zhuǎn)化清洗[3]
根據(jù)不同沉淀溶度積的不同�����,在硫酸鈣中加入碳酸鈉�、磷酸鈉���,使之轉(zhuǎn)化為更易與酸反應(yīng)的碳酸鈣和松軟的磷酸鈣(稱為磷酸鈉的剝離作用)���。因此,在含有難溶物的溶液中加人適量的沉淀轉(zhuǎn)化劑�����,使溶液中的某種離子結(jié)合成為更難溶的物質(zhì)�。
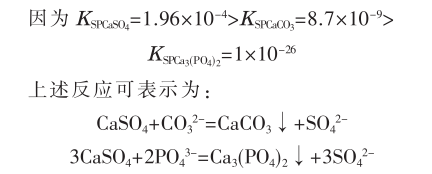
(2)絡(luò)合清洗
在水質(zhì)中加入絡(luò)合劑,使沉積的硫酸鹽垢中的陽離子被絡(luò)合��,從而使沉積物慢慢轉(zhuǎn)移到溶液中��,即達到了清洗的目的。常用的絡(luò)合劑為易溶的乙二按四乙酸二鈉鹽即EDTA,由于鈣�����、鎂離子與EDTA很易形成非常穩(wěn)定的易溶的絡(luò)離子:
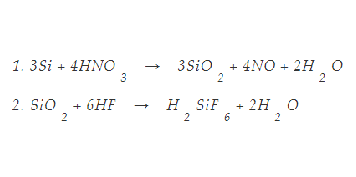
其中Y是EDTA的縮寫孫純賓等叫將HEDP和EDTA兩步絡(luò)合法��,用于清洗電����!中壓鍋爐的硫酸鹽垢�,清洗結(jié)果符合電力部標(biāo)準(zhǔn)的要求。
(3)水溶性高分子絡(luò)合
水溶性高分子化合物的特點是其骨架上帶有
極性基團(如羥基���、氨基�����、竣基�、黃酸基等),這些極性基團能離解出離子�,與溶液中的其它離子進行交換。如磺化交聯(lián)聚苯乙烯樹脂���,其骨架上帶有磺酸基����,在水溶液中能離解出氫離子H+而與水中的Na+、Mg2+�����、Ca2+等陽離子進行交換��。通過交換降低離,子濃度����,減少沉淀的生成。
2.3硅垢和硅酸鹽垢
2.3.1硅垢和硅酸鹽垢的成因
硅酸鈣是灰白色的堅硬的固體���,其傳熱系數(shù)很小�。當(dāng)水中二氧化硅的含量比較高且水的硬度較大時���,比較容易集結(jié)形成硅酸鈣和硅酸鎂垢����。當(dāng)水的pH值較小時�,低硬度水中或水中僅有SiO32-存在時,會產(chǎn)生硅垢���,即膠狀難溶的化合物SiO2·nH2O�。典型的化學(xué)反應(yīng)方程式為:
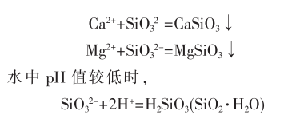
2.3.2清洗機理及方法
(1)酸洗
用一定濃度的HCI和0.5%~10%的氟化物加緩蝕劑進行清洗,反應(yīng)如下:
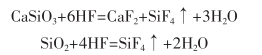
(2)堿洗
如果SiO2的含量在70%~80%以上����,可以直接用15%的NaOH溶液處理,溫度為70℃以上���,視結(jié)垢程度來控制清洗時間。其反應(yīng)為:
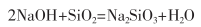
馬文靜等百對電廠含硅酸鹽和銅氧化物的復(fù)合垢進行化學(xué)清洗�,找到了一條堿煮一水沖洗一氧化絡(luò)合除銅一堿沖洗——酸洗——漂洗—氨沖洗—鈍化的清洗和預(yù)膜工藝,取得滿意的效果����。孫克敏回則采用混酸清洗化肥廠鍋爐的硅垢,其配方由主酸�����、補酸���、緩蝕劑��、溶垢促進劑�����、潤濕劑和滲透劑構(gòu)成�,成本低廉。
2.4硫垢和硫化物垢
硫垢屬于一類特殊的垢����,一般只產(chǎn)生在石油或化工裝置的含硫尾氣的治理部分,主要由硫化氫氣體經(jīng)過氧化而形成:
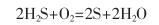
2.4.1硫垢的清洗
因為堿金屬或堿土金屬硫化物的溶液能與單質(zhì)硫發(fā)生反應(yīng)而生成易溶的多硫化物�����,因此一般采用20g/L的Nas飽和溶液��,加特殊的表面活性劑來溶解硫垢�����。反應(yīng)如下:
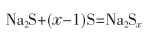
?
多硫化物的溶液一般顯黃色��,隨著x增加����,即硫的含量增加,由黃色變至紅色�?����?筛鶕?jù)結(jié)垢的程度重復(fù)清洗過程�����。
2.4.2煉油廠硫化物的清洗
在堿性條件下��,使硫化物發(fā)生氧化作用(用10%NaOH和5%KMnO4),使其轉(zhuǎn)化為鐵的氫氧化物�����、硫及MnO2沉淀��,再采用10%的HCI進行清洗。
為防止清洗過程中產(chǎn)生CI2,需在HCI中加入少量的醋酸[3]�����。
2.5磷酸鹽垢
2.5.1磷酸垢的形成
水中所含的磷酸鹽濃度很小�����,然而在工業(yè)循環(huán)水中����,由于使用的水處理藥劑中�����,普遍含有無機磷酸鹽����,如磷酸鈉或六偏磷酸鈉�����、有機磷酸(如HEDP�����、PBTC等)作為緩蝕劑��,這些磷酸鹽會與水中的鈣����、鎂離子形成磷酸鹽垢。磷酸鈣垢為灰白色��,當(dāng)設(shè)備受腐蝕時���,磷酸鈣垢中混雜鐵的氧化物��,使水垢由灰白色變成粉紅色�����、紅褐色或黑褐色�����。其反應(yīng)為:2Ca2++3PO43-=Ca2(PO4)3↓
2.5.2磷酸鈣垢清洗
磷酸鈣垢的清洗通常采用氨基磺酸法����。該法所用清洗劑由氨基磺酸、緩蝕劑���、表面活性劑和水組成���。清洗液為酸性��,能與金屬氧化物�、氫氧化物、碳酸鹽反應(yīng)���,生成可溶性鹽類���,從而可除去水垢和鐵銹���。化學(xué)反應(yīng)式為181:
Ca3(PO4)2+6NH2SO3H=3Ca(NH2SO3)2+2H3PO4
2.6金屬氧化物垢
2.6.1鋼鐵的銹垢
(1)銹垢的形成
通常��,暴露在自然環(huán)境中的鋼鐵表面都有由空氣中的水及其電解質(zhì)形成的電解質(zhì)溶液���,這些電解質(zhì)溶液與鋼材中的鐵元素和碳元素形成了無數(shù)微型原電池���。電化學(xué)反應(yīng)的速度很快,是鋼材腐蝕的主要原因�;化學(xué)腐蝕是次要原因。腐蝕的結(jié)果是形成以+2���、+3價鐵的氧化物或氫氧化物為主的復(fù)雜的氧化物�,有時還有少量鐵鹽�。
(2)銹垢的清洗
鋼鐵銹垢一般都溶于酸,反應(yīng)如下:
Fe2O3+6H+=2Fe3++3H2O
2FeO+4H+=Fe3++Fe2++2H2O
Fe3O4+8H+=3Fe2++4H2O
鐵銹垢一般用酸洗��?���?梢杂脽o機酸���,也可以用有機酸,根據(jù)實際情況選擇�。在清洗的時候要注意加入適當(dāng)?shù)木徫g劑和控制清洗時間。
在利用酸洗清洗鋼鐵垢時�,要充分考慮鋼材的組成,并考慮不同酸對鋼材的溶解能力���,以找到合適的清洗劑配方�,文獻[9]介紹了不同無機和有機酸對鋼材鐵的溶解能力�����,對于尋找適宜的清洗劑配方大有益處���。尚世海[101介紹了一種用王水都難以清洗的鐵垢的三步清洗方法����。首先進行熱堿(由NaOH�����、KMnO4��、Na2SiO3,表面活性劑��、滲透劑和緩蝕劑組成循環(huán)�,然后進行酸液(組成為HNO3、尿素和硫脈等)循環(huán)�����,已經(jīng)清洗掉50%的鐵垢�����,其他鐵垢也已松軟�,最后輔以人工清洗,取得了良好效果�。
2.6.2鋁及鋁合金的銹垢
鋁垢的主要成分是組成非常復(fù)雜的水合氧化
鋁和堿式碳酸鋁,主要是由新鮮的鋁表面與空氣氧化形成的�。錯垢的清洗方法是由錯及其氧化物的兩性決定的,一般有酸洗和堿洗兩種方法
(1)酸洗
在清洗的時候應(yīng)盡量采用可以使鋁處于鈍化狀態(tài)的一定濃度的氧化性酸�����,如硝酸,或在清洗液中加人適當(dāng)?shù)木徫g劑���,以減輕酸對機體的腐蝕���。
AL2O3+6H+=2A13++3H2O
(2)堿洗法
采用10%的NaOH即可溶解鋁表面的氧化物,但時間不宜過長���,一般控制在1~2min,以免對基體造成損傷�����。在堿液中添加20~30g/L的NaCl或NaF,可改善清洗表面的外觀�����,注意在清洗中應(yīng)加人適當(dāng)?shù)木徫g劑����。
2.6.3銅及銅合金的銹垢
在潮濕的空氣中����,銅受氧、水�����、二氧化碳和氯化物等作用���,生成堿式碳酸銅或氯化銅等���;當(dāng)受硫化物和氧作用時,則生成棕色或黑色的硫化物垢銅垢的清洗多采用無機酸洗法��,通常采用硝酸�、硫酸和鹽酸的混合酸。應(yīng)根據(jù)實際情況���,采用不同的混酸組合和配比
3有機物類垢的形成及清洗
3.1油垢的形成與清洗
3.1.1油垢類型及成因
型�、成因及其清洗方法�����,見表2��。從表2中可以看出���,溫度是影響油垢類型的主要因素���。隨著溫度升高���,油垢類型從清油垢逐漸轉(zhuǎn)化成焦炭垢。焦炭垢一旦形成并徹底炭化�,其清洗是非常困難的。因此��,對于溫度較高的石化設(shè)備��,要定期清洗����,防止垢的炭化。

3.1.2油垢的清洗
①堿洗����。根據(jù)相似相溶原理,油是憎水化合物��,因此無法采用水洗的方法����。而堿溶液對油污具有較好的親和性,因此�,常用堿性水溶液���,有氫氧化鈉、碳酸鈉�����、磷酸鈉與硅酸鈉等清洗油垢�,一般總是幾種堿組成的堿液清洗劑�����。但是一般堿性清洗液對動物油起皂化反應(yīng)清洗能力好�,而對礦物油清除能力除硅酸鈉外,大多較差�����,因而常作傳統(tǒng)的日用除油劑�,工業(yè)上僅用于一般脫脂。文獻[12]介紹了一種發(fā)動機積炭的清洗方法�����,采用金屬清洗劑��、焦磷酸鈉、苛性鈉����、碳酸鈉、硅氟酸鈉���、銘酸等藥劑構(gòu)成對積炭滲透能力極強的清洗劑�,輔之適當(dāng)?shù)臏囟?�,對發(fā)動機積炭具有理想的清洗效果�。
酸洗。梁小強[13]紹了一種酸性除油垢方
法����。他根據(jù)T-roumg方程選擇合適的清洗劑,即選用與金屬界面張力較低的表面活性劑��,而且愈低愈好��,通過表面活性劑的潤濕力和滲透力把金屬表面的油污潤濕��,使油污松軟��,達到清洗之目的���。據(jù)此�����,設(shè)計了一種由磷酸和烷基酰胺構(gòu)成的油垢清洗劑�����,對油罐的污垢清洗效果良好�。高晶榮等(14)采用復(fù)合酸-有機溶劑復(fù)合清洗劑�����,也取得了理想效果
③有機溶劑法�。常用的有石油類溶劑、鹵代煉溶劑�����、醇類溶劑等�,靠對油類較強的溶解反應(yīng)清除油垢、焦油垢與焦炭垢�。焦炭垢一旦形成并沉積于管壁�,由于附著力極強�����,其清洗是非常困難的����,對于沉積較厚的焦炭垢,可采用溶劑浸潤加機械的辦法���。此外�,近年來開發(fā)的超聲波等方法具有一定效果����,但成本昂貴
①表面活性劑法表面活性劑由于具有兩親結(jié)構(gòu)(親水基和親油基),因而其低濃度水溶液具有減少表面張力、潤濕滲透��、乳化分散和增溶等獨特作用���,故對液態(tài)油垢具有良好的去除能力��,但對固態(tài)油垢去除能力差����。
⑤氧化法���。選用濃硫酸�����、硝酸與銘酸等強氧化性酸能較好地清除焦油垢�、膠垢與積炭垢,以及含硫化鐵的油垢�。但這些強氧化型清洗劑,雖在常溫下操作����,但稍有不慎就會造成事故。銘酸還存在排污公害的問題�。
⑥復(fù)合法。對于工業(yè)油污油垢���,很少局限于一種類型,因此�����,單獨采用一種清洗方法往往難以徹底清除油污油垢��,這樣就需要根據(jù)實際情況���,聯(lián)合采用多種方法進行清洗����。將絡(luò)合劑、堿性溶液�、表面活性劑等不同物質(zhì)混合起來,發(fā)揮各自的優(yōu)勢��,具有更好的除垢能力����。
⑦干冰法。唐純[15]紹了利用干冰清洗導(dǎo)熱
油爐的方法�。這是一種物理除垢法,其主要原理是利用干冰的低溫(-78℃)使灰垢被冷凍至脆化及爆裂����,而達到清除積垢的目的,實踐證明利用干冰清洗不留死角�,清除效率高
3.2糖垢的形成和清洗山
糖垢也稱為碳水化合物垢,是由無機物和有機物構(gòu)成的����,通常由蔗糖、蔗蠟、碳酸鈣�����、亞硫酸鈣��、硅酸鈣�、草酸鈣、蛋白質(zhì)等組成的�,因制糖工藝的不同而有變化在糖什蒸發(fā)和濃縮的過程中,在多效蒸發(fā)罐的一效蒸發(fā)罐壁上首先析出溶解度較小的碳酸鎂��、碳酸鈣�、磷酸鈣以及焦化物,再析出溶解度較大的硫酸鈣�、亞硫酸鈣、檸撐酸鈣和草酸鈣等糖汁中可溶的有機和九機鈣鹽����,通過與糖汁中的碳酸離子反應(yīng),轉(zhuǎn)化為不溶性的碳酸鈣鹽沉淀�����。其中的可溶性無機鈣鹽�,如碳酸鈣、亞硫酸鈣等受熱分解成為難溶的碳酸鈣垢��。糖汁中的金屬氧化物和氫氧化物膠狀物��,在糖汁的濃縮過程中會析出���。酸性的糖汁對設(shè)備也會腐蝕�����,生成金屬氧化物垢和鹽垢����。此外在制糖工藝中加入的一些助劑也會成為糖垢的組成成分����。糖垢的清洗方法應(yīng)根據(jù)糖垢的組成采取上述無機垢或油垢的清洗方法。